REGARD D’EXPERT 8 novembre 2023
Il est là, sous nos pieds : le sol. On le regarde à peine, pourtant c’est sous la terre que sont stockées les plus grandes quantités de carbone des écosystèmes terrestres. Les sols peuvent jouer un rôle substantiel pour réduire les concentrations de gaz à effets de serre dans l’atmosphère. Via la préservation des stocks importants de carbone souterrain, d’une part, mais aussi par la restauration des terres dégradées notamment grâce à certaines pratiques agricoles, qui permettent de piéger davantage de carbone sous la terre, voici comment.

Lire aussi
Carbone des sols : un panorama mondial des impacts des activités humaines
L’agroforesterie peut jouer un rôle clé dans la lutte contre le changement climatique
A écouter
Capturer le CO2 : la solution miracle ?
Un podcast AFP-The conversation
Rémi Cardinael
Cirad, Zimbabwe
Dans notre vie quotidienne on le regarde à peine, et pourtant, il ne s’agit rien de moins que du plus grand stock de carbone des écosystèmes terrestres. Ce palmarès ne revient en effet pas aux forêts, ni à l’atmosphère, mais bel et bien aux sols. On trouve environ 2400 milliards de tonnes de carbone dans les deux premiers mètres de profondeur sous la terre, soit trois fois plus que ce que l’on trouve dans l’atmosphère.
À l’heure du dérèglement climatique et de la nécessité absolue de réduire les émissions de gaz à effet de serre, cette impressionnante capacité des sols à stocker du carbone laisse songeur. Si les sols ne pourront bien entendu pas à eux seuls faire baisser drastiquement les concentrations de gaz à effets de serre dans l’atmosphère qui sont responsables du réchauffement climatique, ils peuvent néanmoins jouer un rôle substantiel, via la préservation des stocks importants de carbone souterrain, mais aussi via la restauration des terres dégradées notamment grâce à certaines pratiques agricoles, qui permettent de piéger davantage de carbone sous la terre.
Comment le carbone entre dans les sols
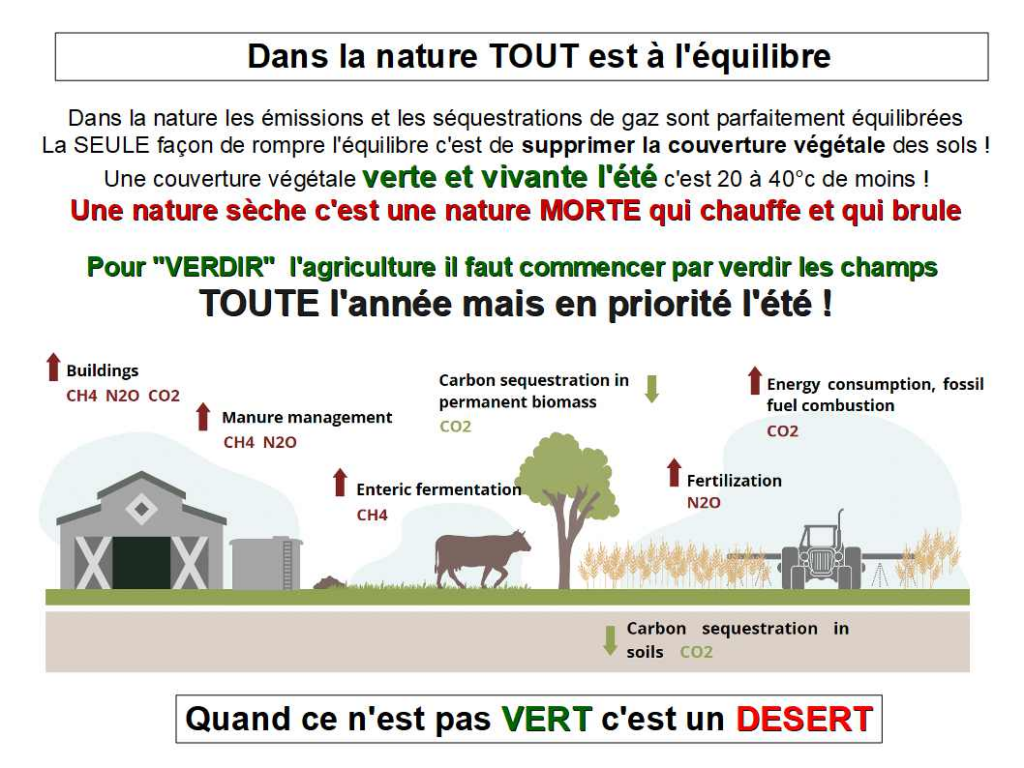
Tout commence par la photosynthèse : au cours de celle-ci, les plantes fixent du dioxide de carbone (CO2) atmosphérique au sein de chloroplastes, de petits organites cellulaires riches en chlorophylle. Le CO2 est associé à des molécules d’eau (H20) grâce à l’énergie solaire, et produit ainsi des glucides (molécules riches en carbone) et de l’oxygène (O2). Une partie de ce carbone capté par la plante arrive directement dans le sol via les racines des végétaux, à la fois par l’exsudation racinaire et par le renouvellement des racines fines.
Du carbone peut également entrer dans les sols lorsque les feuilles mortes d’une plante tombent, ou quand les résidus de culture sont laissés sur le champ. Une fois tombées, ces feuilles mortes riches en carbone tapissent le sol, se décomposent, sont ingérées par des bactéries, champignons ou vers de terre et finissent par se transformer en matières organiques des sols. Des animaux peuvent également accélérer ce processus de transfert du carbone dans le sol par exemple, les termites champignonnistes, qui transportent des résidus de végétaux dans leurs termitières où une symbiose avec des champignons leur permet de les rendre plus assimilables pour celles-ci.
Certaines régions et écosystèmes possèdent des stocks de carbone des sols très importants. C’est le cas par exemple des régions boréales, où des stocks énormes sont préservés dans le permafrost mais aujourd’hui menacés par le réchauffement climatique. Dans les régions tropicales, la productivité importante des écosystèmes notamment forestiers, ainsi que des sols très profonds, expliquent aussi les stocks importants observés.
L’enjeu principal pour tous ces écosystèmes riches en carbone tels que les forêts, les zones humides, les mangroves ou encore les prairies permanentes est le maintien de ces stocks plus que leur augmentation, car ce carbone est considéré comme irrécouvrable à l’échelle humaine. Cela passe par un arrêt de la déforestation et de la conversion des écosystèmes en terres cultivées. En moyenne, 25 % du carbone du sol est perdu lorsque des forêts ou des zones humides sont converties en terres cultivées, parfois plus. Sur les terres agricoles, certaines pratiques permettent de séquestrer plus de carbone dans les sols. Généraliser leur utilisation est un des objectifs de l’initiative baptisée « 4 pour 1000 » lancée à l’occasion de la COP21.
Quelles pratiques agricoles augmentent le stock de carbone des sols ?
De nombreuses pratiques permettent d’augmenter les stocks de carbone des sols agricoles, comme l’agroforesterie, les couverts intermédiaires, ou encore les amendements organiques. Parmi les solutions souvent mises en avant, trois reviennent régulièrement. La première est le non-labour ou la réduction du travail du sol. Cette technique consiste à semer les cultures sans que l’intégralité du champ n’ait été travaillée ou labourée, au préalable. Cette pratique permet de réduire l’érosion du sol, de ralentir la décomposition des matières organiques par une moindre oxygénation du sol, de préserver sa biodiversité (notamment les vers de terre).
%20appliqu%C3%A9s%20%C3%A0%20la%20surface%20apr%C3%A8s%20la%20r%C3%A9colte.%20R%C3%A9mi%20Cardinael.JPG)
La deuxième pratique promue est celle de la couverture permanente des sols, soit avec des paillis issus des résidus de culture laissés sur le champ, soit par des couverts végétaux vivants entre les différentes cultures. Cette couverture des sols les protège contre l’érosion notamment hydrique, permet de fixer du carbone tout en étant bénéfique pour la faune du sol (bactéries, champignons, lombrics…).
La troisième technique promue est celle de la diversification des cultures, soit en rotation, soit en association. Cette diversification permet de limiter le développement des bioagresseurs et maladies des plantes, mais aussi d’augmenter la productivité des parcelles cultivées notamment grâce à des effets précédents des cultures. Par exemple, une légumineuse (pois, haricot, arachide, féverole, luzerne…) dans la rotation va fixer de l’azote de l’air et le rendre disponible dans le sol pour la culture suivante, favorisant ainsi sa croissance. Une meilleure productivité des cultures permet d’avoir plus de carbone fixé sur la parcelle, et donc plus de carbone dans les sols, notamment via les racines des cultures.
Ces trois pratiques correspondent aux trois piliers de ce que l’on appelle « l’agriculture de conservation ». Ces pratiques deviennent réellement efficaces pour augmenter le carbone des sols lorsqu’elles sont associées. Pratiquées seules, elles n’ont parfois que peu ou pas d’impact. C’est notamment le cas du non-labour seul, qui peut avoir un effet positif sur le carbone des sols dans certains contextes mais pas dans d’autres. La communauté scientifique a mis du temps à s’en rendre compte car les travaux se sont d’abord surtout focalisés sur les premiers centimètres du sol qui, sous l’effet du non-labour, avaient effectivement une plus forte teneur en carbone.
Mais cela s’accompagnait parfois d’une réduction du carbone du sol dans les couches plus profondes par rapport à des systèmes labourés où le carbone du sol est homogénéisé sur 20 ou 30 cm de profondeur. Le non-labour a donc, dans certains cas, surtout un effet sur la redistribution du carbone dans le profil de sol, sans nécessairement conduire à une augmentation nette du stock sur son ensemble, ce qui est nécessaire quand on s’intéresse à l’atténuation du changement climatique. Une synthèse récente de travaux menés en Afrique subsaharienne suggère que seule la combinaison des trois piliers de l’agriculture de conservation permet d’augmenter significativement les stocks de carbone des sols, la réduction du travail du sol seule étant inefficace.
Quels résultats au Zimbabwe et au Cambodge ?
Pour bien comprendre les bénéfices de ces trois pratiques quand elles sont associées, il est crucial d’avoir des expérimentations sur le long cours. Il faut en effet compter en moyenne 5 à 10 ans pour qu’une variation de stock de carbone du sol soit détectée de façon significative.
Au Cambodge, le Cirad et le ministère de l’agriculture du Cambodge ont démarré des expérimentations il y a quatorze ans, sur des systèmes à base de manioc, une culture couvrant près de 700 000 hectares dans le pays et principalement destinée à l’exportation pour produire de la farine pour l’alimentation animale.
En couplant le non-travail du sol et du semis direct, la couverture permanente des sols avec des couverts végétaux, et la rotation des cultures avec du maïs, nous avons pu noter une hausse importante de carbone dans les sols, avec des taux d’accumulation du carbone de l’ordre de 0,7 à 0,8 tonnes de carbone par hectare et par an jusqu’à 40 cm de profondeur. Le climat chaud et humide de la région permet en effet une couverture permanente des sols avec des couverts végétaux très productifs incluant des légumineuses (crotalaire, niébé) et des graminées (mil) entre la culture du manioc et du maïs, sur lesquels on sème le maïs.
Ce faisant, du carbone est fixé toute l’année par la photosynthèse, et un système racinaire très profond se développe permettant d’augmenter les stocks de carbone au-delà des premières strates du sol. Ce stockage de carbone additionnel dans le sol va continuer jusqu’à ce qu’un nouvel équilibre du système soit atteint. Cet essai a vocation à être maintenu dans la durée pour estimer pendant combien de décennies un tel système permet de stocker du carbone. Une fois l’équilibre atteint, l’enjeu sera alors la préservation de ces stocks de carbone par le maintien des bonnes pratiques de gestion des sols. Bien gérer les sols suppose une gestion sur la durée plutôt que par à-coup.
Au Zimbabwe, dans un contexte totalement différent, avec une saison sèche de sept mois et une saison des pluies de cinq mois, nous avons voulu également mesurer l’efficacité de ces pratiques couplées sur le long terme. Nous disposons pour cela d’un essai mis en place par nos collègues du Centre International d’Amélioration du Maïs et du Blé il y a dix ans dans un système bas-intrant avec pour culture principale le maïs. Nous avons pu mesurer les stocks de carbone du sol des différentes pratiques, seules ou associées : des champs avec du travail du sol, des champs sans travail du sol, avec ou sans résidu de culture du maïs (paillis), et avec ou sans rotation avec le niébé, une légumineuse.
Encore une fois, les résultats montrent que le non-travail du sol seul ne peut pas grand chose, il induit même une légère perte de carbone du sol par rapport à un travail du sol. Cela est expliqué sur ce site par la plus forte compaction du sol quand celui-ci n’est pas travaillé, les racines donc ont du mal à se développer. De plus, la pluie pénètre moins bien et ruisselle sur le sol, ce qui entraîne des stress hydriques sur le maïs. Au final, le maïs se développe beaucoup moins bien dans ces systèmes, il y a donc moins d’apport de carbone au sol par les racines, ce qui se traduit par une perte de carbone des sols.
En revanche, les champs sans travail du sol avec un paillis de résidus de culture de maïs de la saison précédente et une rotation des cultures permettent eux d’augmenter les stocks de carbone, avec, cependant, un effet limité à l’horizon de surface. On observe cependant une augmentation nette du stock de carbone car aucune perte de carbone en profondeur n’a été observée.
Quels obstacles au développement de ces pratiques ?

Si ces résultats sont prometteurs, ces pratiques ne sont pour autant pas toujours faciles à mettre en place. Au Zimbabwe, par exemple, une contrainte majeure apparaît. Les systèmes agricoles sont des systèmes de polyculture-élevage à bas-intrant (peu de fertilisation minérale, peu ou pas de mécanisation). À la récolte, seuls les épis de maïs sont récoltés, à la main, et les tiges de maïs restent debout dans le champ. Celles-ci serviront de nourriture au bétail pendant la saison sèche où les vaches viennent pâturer directement dans les champs, après avoir vagabondé dans les forêts et zones communales pendant la saison humide.
Il y a donc une compétition d’usage pour les résidus de maïs, pour nourrir le bétail ou pour couvrir les sols. Certains agriculteurs installent des clôtures afin que le bétail ne vienne pas manger les résidus durant la saison sèche, ce qui a un coût. D’autres les récoltent et les entreposent en hauteur, à l’abri des bêtes, et apportent le paillis à l’approche de la saison humide. Cela suppose toute une organisation, du temps et de l’énergie supplémentaires. Dans les deux cas, il faut également trouver une source d’alimentation alternative pour le bétail.
Sur ces terrains comme sur d’autres, l’intérêt de ces pratiques pour les agriculteurs ne réside donc pas dans la séquestration de carbone dans les sols et de son impact sur l’atténuation du changement climatique. Ces techniques sont surtout plébiscitées pour leur impact positif sur la fertilité des sols et la productivité des cultures qui en découle, en réduisant le risque d’érosion, en améliorant la disponibilité des nutriments mais aussi en permettant de s’adapter au changement climatique à travers par exemple une meilleure conservation de l’eau. Ces bénéfices sont cruciaux et bien souvent prioritaires pour les agriculteurs du Sud Global, qui sont parmi les plus impactés par le changement climatique.













 Ouvrir en mode plein écran
Ouvrir en mode plein écran Ouvrir en mode plein écran
Ouvrir en mode plein écran Ouvrir en mode plein écran
Ouvrir en mode plein écran