James J. Hoorman, cultures de couverture et qualité de l’eau, éducateur en vulgarisation, vulgarisation de l’Ohio State UniversityRafiq Islam, spécialiste des sols et de l’eau, Ohio State University Extension, South Centers at Piketon
Les micro-organismes du sol existent en grand nombre dans le sol tant qu’il existe une source de carbone pour l’énergie. Il existe un grand nombre de bactéries dans le sol, mais en raison de leur petite taille, leur biomasse est plus faible. Les actinomycètes sont 10 fois plus petits en nombre, mais sont plus grands en taille et ont donc une biomasse similaire à celle des bactéries. Les populations de champignons sont plus petites mais dominent la biomasse du sol lorsque le sol n’est pas perturbé. Les bactéries, les actinomycètes et les protozoaires sont robustes et peuvent tolérer davantage de perturbations du sol que les populations fongiques. Ils dominent donc dans les sols labourés, tandis que les populations fongiques et nématodes ont tendance à dominer dans les sols labourés ou sans labour.
Il y a plus de microbes dans une cuillère à café de terre qu’il n’y a d’habitants sur terre. Les sols contiennent environ 8 à 15 tonnes de bactéries, champignons, protozoaires, nématodes, vers de terre et arthropodes. Voir les fiches d’information sur les rôles des bactéries, des champignons, des protozoaires et des nématodes du sol.
| Tableau 1 : Nombre relatif et biomasse des espèces microbiennes à une profondeur de sol de 0 à 6 pouces (0 à 15 cm) | ||
| Microorganismes | Nombre/g de sol | Biomasse (g/m 2 ) |
| Bactéries | 10 8 –10 9 | 40 à 500 |
| Actinomycètes | 10 7 –10 8 | 40 à 500 |
| Champignons | 10 5 –10 6 | 100-1500 |
| Algues | 10 4 –10 5 | 1 à 50 |
| Protozoaires | 10 3 –10 4 | Varie |
| Nématodes | 10 2 –10 3 | Varie |
Décomposition microbienne de la matière organique du sol
La décomposition de la matière organique remplit deux fonctions pour les micro-organismes : fournir de l’énergie pour la croissance et fournir du carbone pour la formation de nouvelles cellules. La matière organique du sol (MOS) est composée des fractions « vivantes » (micro-organismes), « mortes » (résidus frais) et « très mortes » (humus). Le « très mort » ou humus est la fraction de MOS à long terme, vieille de plusieurs milliers d’années et résistante à la décomposition. La matière organique du sol contient deux composants appelés MOS active (35 %) et passive (65 %). La MOS active est composée de matières végétales ou animales fraîches « vivantes » et « mortes » qui servent de nourriture aux microbes et sont composées de sucres et de protéines faciles à digérer. La SOM passive est résistante à la décomposition par les microbes et est plus riche en lignine.
Les microbes ont besoin d’un apport régulier de MOS active dans le sol pour survivre dans le sol. Les sols non labourés à long terme contiennent des niveaux de microbes nettement plus élevés, plus de carbone actif, plus de MOS et plus de carbone stocké que les sols labourés conventionnels. La majorité des microbes présents dans le sol existent dans des conditions de famine et ont donc tendance à être dans un état dormant, en particulier dans les sols labourés.
Les résidus végétaux morts et les éléments nutritifs des plantes deviennent la nourriture des microbes présents dans le sol. La matière organique du sol (MOS) correspond essentiellement à toutes les substances organiques (tout ce qui contient du carbone) présentes dans le sol, vivantes et mortes. La MOS comprend les plantes, les algues bleu-vert, les micro-organismes (bactéries, champignons, protozoaires, nématodes, coléoptères, collemboles, etc.) et la matière organique fraîche et en décomposition provenant des plantes, des animaux et des micro-organismes.
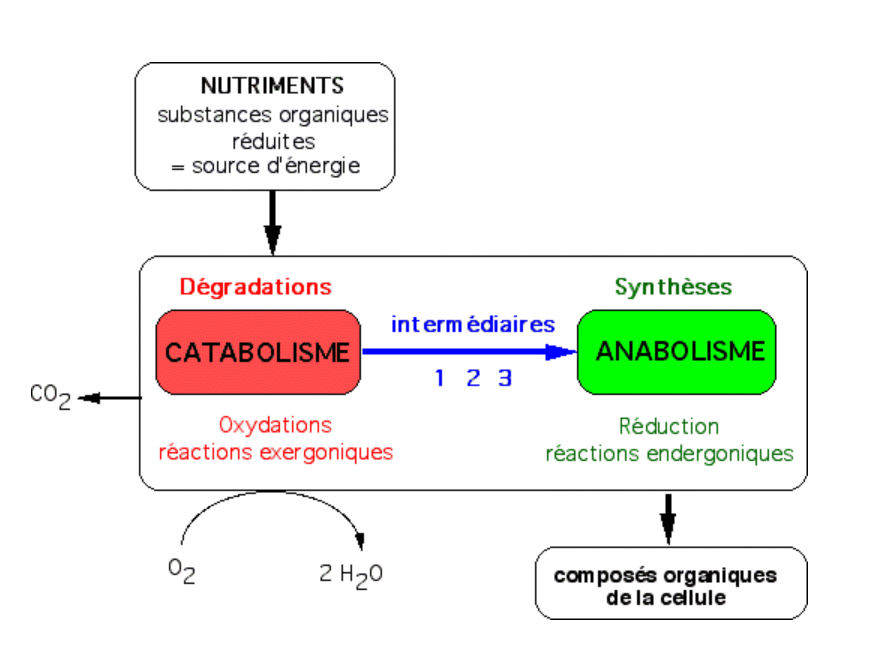
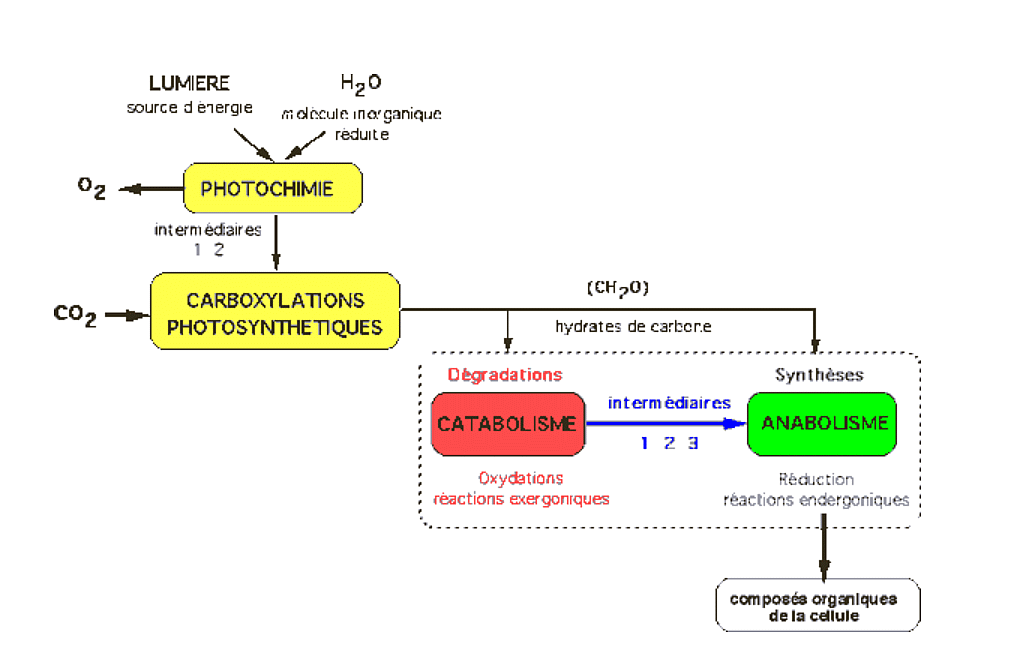
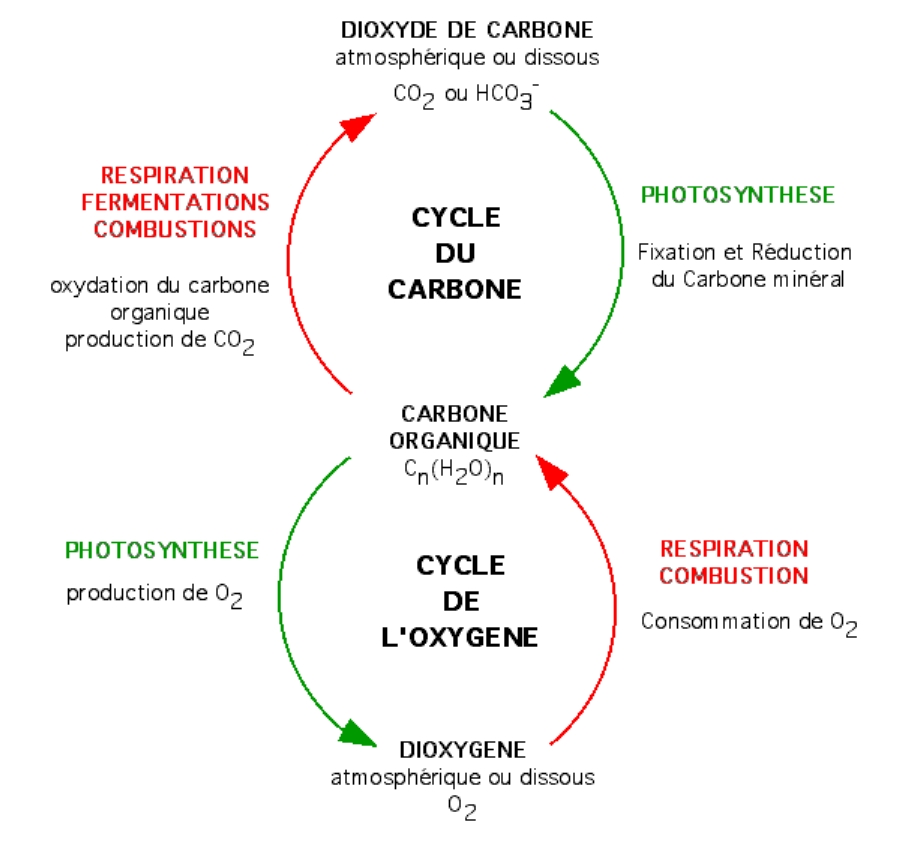
La matière organique du sol peut être décomposée en ses éléments constitutifs. Cent grammes (g) ou 100 livres (lbs) de matière végétale morte produisent environ 60 à 80 g (lbs) de dioxyde de carbone, qui est rejeté dans l’atmosphère. Les 20 à 40 g (lb) d’énergie et de nutriments restants sont décomposés et transformés en environ 3 à 8 g (lb) de micro-organismes (les vivants), 3 à 8 g (lb) de composés non humiques (les morts), et 10 à 30 g (lb) d’humus (la matière très morte, résistante à la décomposition). La structure moléculaire de la MOS est principalement constituée de carbone et d’oxygène avec un peu d’hydrogène et d’azote et de petites quantités de phosphore et de soufre. La matière organique du sol est un sous-produit des cycles du carbone et de l’azote.

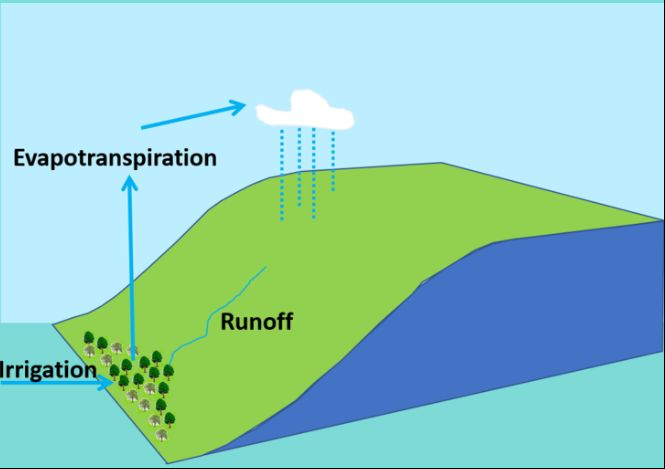
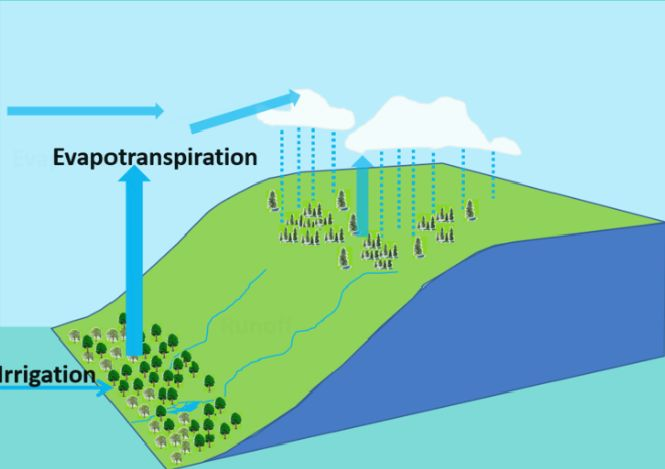
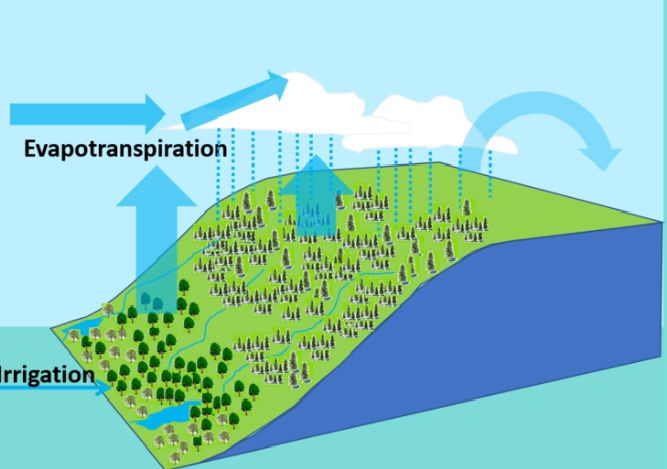
Figure 1. Diagramme du Dr Rafiq Islam.
Nutriments de la matière organique du sol
Les éléments nutritifs du sol ont une valeur actuelle de 680 $ pour chaque 1 pour cent de MOS ou de 68 $ par tonne de MOS sur la base des valeurs économiques des engrais commerciaux (voir tableau 2). La MOS est composée principalement de carbone, mais associée au carbone sont de grandes quantités d’azote et de soufre provenant des protéines, du phosphore et du potassium. Le SOM doit être considéré comme un investissement dans un certificat de dépôt (CD). Les sols biologiquement actifs et contenant de plus grandes quantités de carbone actif recyclent et libèrent plus de nutriments pour la croissance des plantes que les sols biologiquement inactifs et contiennent moins de matière organique active. Dans des conditions de culture sans labour, de petites quantités de nutriments sont libérées chaque année (comme les intérêts sur un CD) pour fournir des nutriments lentement et efficacement aux racines des plantes. Cependant, avec le travail du sol, de grandes quantités de nutriments peuvent être libérées puisque la MOS est consommée et détruite par les microbes. Étant donné que les niveaux de MOS mettent du temps à s’accumuler, la capacité de stockage des nutriments est diminuée et les excédents de nutriments libérés sont souvent lessivés dans les eaux de surface. La SOM est un réservoir de nombreux nutriments végétaux.
Considérez les trois scénarios suivants. Les sols renouvellent généralement 1 à 3 pour cent de leur azote stocké dans la MOS. Les sols labourés ou malsains libèrent un pourcentage d’azote plus faible en raison d’une activité microbienne plus faible. Un sol labouré avec 2 pour cent de MOS (2 000 livres de N) peut libérer 1 pour cent de N ou 20 livres de N par an. Un sol plus biologiquement actif et contenant 4 pour cent de MOS (4 000 lb de N) peut libérer 1,5 pour cent de N ou 60 lb de N, tandis qu’un sol à 6 pour cent de MOS (6 000 lb de N) peut libérer 2 pour cent de N ou 120 lb de N. Dans les sols, les excédents de nutriments libérés sont souvent perdus et les réserves de carbone sont épuisées, ce qui réduit le stockage futur des nutriments. Les agriculteurs constatent souvent cela lorsqu’ils labourent un sol vierge, un vieux pâturage ou une clôture. Pendant plusieurs années, les cultures sur le sol nouvellement labouré pousseront mieux que les sols environnants, mais avec le temps, le sol sera épuisé en carbone et le sol nouvellement labouré deviendra moins fertile car le carbone est oxydé sous forme de dioxyde de carbone et perdu dans l’atmosphère. . Le travail du sol entraîne l’oxydation et la destruction du carbone dans le sol en augmentant les niveaux d’oxygène du sol, favorisant ainsi l’expansion des populations de bactéries et la consommation de carbone actif dans le sol.
| Tableau 2 : Valeur de la matière organique du sol | |
| Hypothèses : 2 000 000 livres de sol dans les 6 premiers pouces | |
| Nutriments | 1% de matière organique = 20 000# 50%Carbone, rapport C:N = 10:1 |
| Azote: | 1000# * 0,50$/#N = 500$ |
| Phosphore: | 100# * 0,70$/#P = 70$ |
| Potassium: | 100# * 0,40$/#K = 40$ |
| Soufre: | 100# * 0,50$/#S = 50$ |
| Carbone: | 10 000# ou 5 tonnes * 4 $/tonne = 20 $ |
| Valeur de 1 % de nutriments SOM/acre | = 680 $ |
| Rapport relatif des nutriments : | 100 Carbone/10 Azote/ 1 Phosphore/1 Potassium/1 Soufre |
Effets du climat, de la température et du pH sur la MOS
La MOS est affectée par le climat et la température. Les populations microbiennes doublent à chaque changement de température de 10 degrés Fahrenheit. Si nous comparons les tropiques aux régions arctiques plus froides, nous constatons que la majeure partie du carbone est retenue dans les arbres et la végétation aérienne. Sous les tropiques, la couche arable contient très peu de MOS car les températures élevées et l’humidité décomposent rapidement la MOS. En se déplaçant vers le nord ou le sud de l’équateur, la MOS augmente dans le sol. La toundra près du cercle polaire arctique contient une grande quantité de MOS en raison des températures froides. Les températures glaciales modifient le sol de sorte qu’une plus grande quantité de MOS est décomposée que dans les sols non sujets au gel.
L’humidité, le pH, la profondeur du sol et la taille des particules affectent la décomposition de la MOS. Les régions chaudes et humides stockent moins de carbone organique dans le sol que les régions sèches et froides en raison d’une décomposition microbienne accrue. Le taux de décomposition de la MOS augmente lorsque le sol est exposé à des cycles de séchage et d’humidification par rapport aux sols continuellement humides ou secs. Toutes choses étant égales par ailleurs, les sols dont le pH est neutre à légèrement alcalin décomposent la MOS plus rapidement que les sols acides ; par conséquent, le chaulage du sol améliore la décomposition de la MOS et l’évolution du dioxyde de carbone. La décomposition est également plus importante près de la surface du sol, là où se trouvent la plus forte concentration de résidus végétaux. À de plus grandes profondeurs, la décomposition de la MOS est moindre, ce qui correspond à une baisse des niveaux de carbone organique due à la diminution des résidus végétaux. Les petites particules sont plus facilement dégradées par les microbes du sol que les grosses particules, car la surface globale est plus grande avec les petites particules, de sorte que les microbes peuvent attaquer les résidus.
Une différence dans la formation des sols se produit également d’est en ouest à travers les États-Unis. À l’est, les forêts de feuillus prédominaient et les racines pivotantes des arbres étaient riches en lignine, et les arbres à feuilles caduques laissaient de grandes quantités de feuilles mortes à la surface du sol. Les racines des feuillus ne se renouvellent pas rapidement, de sorte que les niveaux de matière organique dans le sous-sol sont assez faibles. Dans les sols forestiers, la majeure partie de la MOS est distribuée dans les quelques centimètres supérieurs. À mesure que vous vous déplacez vers l’ouest, de hautes prairies dominent le paysage et la couche arable se forme à partir de systèmes racinaires profonds et fibreux. Cinquante pour cent des racines d’une herbe meurent et sont remplacées chaque année et les racines de l’herbe sont riches en sucres et en protéines (matière organique active plus élevée) et plus faibles en lignine. Ainsi, les sols formés sous les prairies à herbes hautes sont riches en MOS dans tout le profil pédologique. Ces sols de premier choix sont très productifs car ils ont un pourcentage plus élevé de MOS (en particulier de charbon actif), retiennent plus de nutriments, contiennent plus de microbes et ont une meilleure structure du sol en raison de populations fongiques plus importantes.
Rapport carbone/azote
La dégradation des résidus organiques par les microbes dépend du rapport carbone/azote (C:N). Les microbes présents dans le rumen d’une vache, dans un tas de compost et dans le sol dépendent du rapport C:N pour décomposer les résidus organiques (à base de carbone). Considérez deux sources d’alimentation distinctes, un jeune plant de luzerne tendre et de la paille d’avoine ou de blé. Une jeune plante de luzerne contient plus de protéines brutes, d’acides aminés et de sucres dans la tige, elle est donc facilement digérée par les microbes, que ce soit dans le rumen d’une vache, dans un tas de compost ou dans le sol. La jeune luzerne a une teneur élevée en azote provenant des protéines (les acides aminés et les protéines sont riches en azote et en soufre), elle a donc un rapport carbone/azote plus faible (moins de carbone, plus d’azote). Cependant, la paille d’avoine et de blé (ou le foin plus âgé) contient plus de lignine (qui résiste à la décomposition microbienne), moins de protéines brutes, moins de sucres dans la tige et un rapport C:N plus élevé. La paille est décomposée par les microbes, mais il faut plus de temps et d’azote pour décomposer cette source riche en carbone.
Une faible teneur en azote ou un rapport C:N élevé est associé à une lente décomposition de la MOS. Les plantes immatures ou jeunes ont une teneur en azote plus élevée, des rapports C:N plus faibles et une décomposition plus rapide de la SOM. Pour un bon compostage, un rapport C:N inférieur à 20 permet aux matières organiques de se décomposer rapidement (4 à 8 semaines) tandis qu’un rapport C:N supérieur à 20 nécessite un supplément d’azote et ralentit la décomposition. Ainsi, si nous ajoutons au sol un matériau à haute teneur en carbone et à faible teneur en N, les microbes capteront l’azote du sol. Finalement, l’azote du sol est libéré mais à court terme, l’azote est retenu. Le facteur de conversion pour convertir l’azote en protéines brutes est de 16,7, ce qui explique pourquoi il est si important d’avoir un rapport C:N inférieur à 20.
Le rapport C:N de la plupart des sols est d’environ 10:1, ce qui indique que l’azote est disponible pour la plante. Le rapport C:N de la plupart des résidus végétaux a tendance à diminuer avec le temps, à mesure que la MOS se désintègre. Cela résulte de la perte gazeuse de dioxyde de carbone. Par conséquent, le pourcentage d’azote dans la MOS résiduelle augmente à mesure que la décomposition progresse. Le rapport C:N de 10:1 de la plupart des sols reflète une valeur d’équilibre associée à la plupart des microbes du sol (bactéries 3:1 à 10:1, champignon 10:1 rapport C:N).
Les bactéries sont les premiers microbes à digérer les nouveaux résidus organiques végétaux et animaux présents dans le sol. Les bactéries peuvent généralement se reproduire en 30 minutes et ont une teneur élevée en N dans leurs cellules (3 à 10 atomes de carbone pour 1 atome d’azote ou 10 à 30 pour cent d’azote). Dans de bonnes conditions de chaleur, d’humidité et de nourriture, ils peuvent se reproduire très rapidement. Les bactéries sont généralement moins efficaces pour convertir le carbone organique en nouvelles cellules. Les bactéries aérobies assimilent environ 5 à 10 pour cent du carbone tandis que les bactéries anaérobies n’en assimilent que 2 à 5 pour cent, laissant derrière elles de nombreux déchets composés de carbone et utilisant de manière inefficace l’énergie stockée dans la MOS.

Figure 2. Graphique du N relatif disponible avec la durée de décomposition.
Luzerne, faible rapport C:N, C:N = 13:1
Paille d’avoine, rapport C:N élevé, C:N = 80:1
Les champignons libèrent généralement moins de dioxyde de carbone dans l’atmosphère et sont plus efficaces pour convertir le carbone pour former de nouvelles cellules. Le champignon capte généralement plus d’énergie de la MOS à mesure qu’il la décompose, assimilant 40 à 55 pour cent du carbone. La plupart des champignons consomment de la matière organique plus riche en cellulose et en lignine, dont la décomposition est plus lente et plus difficile. La teneur en lignine de la plupart des résidus végétaux pourrait être plus importante que le rapport C:N pour prédire la vitesse de décomposition.
Les champignons mycorhiziens vivent dans le sol, à la surface ou dans les racines des plantes. Les champignons ont une grande surface et contribuent au transport des nutriments minéraux et de l’eau vers les plantes. Le cycle de vie des champignons est plus complexe et plus long que celui des bactéries. Les champignons ne sont pas aussi résistants que les bactéries et nécessitent une source de nourriture plus constante. Les niveaux de population de champignons ont tendance à diminuer avec le travail du sol conventionnel. Les champignons ont un rapport carbone/azote plus élevé (10:1 carbone/azote ou 10 % d’azote) mais sont plus efficaces pour convertir le carbone en matière organique du sol. Avec des résidus organiques riches en C:N, les bactéries et les champignons extraient l’azote du sol (voir le graphique sur l’immobilisation nette).
Les protozoaires et les nématodes consomment d’autres microbes. Les protozoaires peuvent se reproduire en six à huit heures, tandis que les nématodes mettent de trois jours à trois ans, avec une moyenne de 30 jours pour se reproduire. Après avoir consommé les bactéries ou autres microbes (riches en azote), les protozoaires et les nématodes libèrent de l’azote sous forme d’ammonium (voir le graphique sur la minéralisation nette). L’ammonium (NH 4 +) et les nitrates (NO 3 -) sont facilement convertis dans les deux sens dans le sol. Les plantes absorbent les nitrates d’ammonium et du sol pour se nourrir grâce au réseau mycorhizien des champignons.
Les populations de micro-organismes changent rapidement dans le sol à mesure que les produits SOM sont ajoutés, consommés et recyclés. La quantité, le type et la disponibilité de la matière organique détermineront la population microbienne et son évolution. Chaque organisme individuel (bactéries, champignons, protozoaires) possède certaines enzymes et réactions chimiques complexes qui aident cet organisme à assimiler le carbone. À mesure que des déchets sont générés et que les résidus organiques d’origine sont décomposés, de nouveaux micro-organismes peuvent prendre le relais, se nourrissant des déchets, de la nouvelle communauté microbienne florissante (généralement des bactéries) ou de la MOS plus résistante. Les premiers décomposeurs attaquent généralement les sucres et les protéines faciles à digérer, suivis par les micro-organismes qui s’attaquent aux résidus les plus résistants.

Figure 3. Graphique du niébé (C:N <20) décomposé par les bactéries et les champignons, l’évolution du dioxyde de carbone et les protozoaires et les nématodes consommant les bactéries et les champignons et excrétant de l’ammonium dans le sol pour la croissance des plantes. NO3- et NH4+ sont facilement convertis dans le sol. Graphique du Dr Rafiq Islam.

Figure 4. Graphique du niébé (C:N <20) décomposé par les bactéries et les champignons, l’évolution du dioxyde de carbone et les protozoaires et les nématodes consommant les bactéries et les champignons et excrétant de l’ammonium dans le sol pour la croissance des plantes. NO3- et NH4+ sont facilement convertis dans le sol. Graphique du Dr Rafiq Islam.
Les cultures de couverture fournissent de la nourriture (carbone actif comme le glucose et les protéines) aux microbes dont ils peuvent se nourrir. Dans le sol, il y a 1 000 à 2 000 fois plus de microbes associés aux racines que ceux vivant dans un sol nu ou labouré. Les microbes fabriquent à leur tour de la MOS et stockent les nutriments du sol. La construction de SOM nécessite que les éléments nutritifs du sol comme le NPKS soient liés dans le sol. Les cultures de couverture hivernales absorbent l’excès de nutriments du sol et fournissent de la nourriture à tous les microbes présents dans le sol pendant les mois d’hiver, plutôt que d’utiliser les réserves de MOS pour les nutriments. Dans un champ labouré conventionnel, les éléments nutritifs du sol sont rapidement libérés à mesure que la MOS est brûlée et que l’habitat des microbes et des organismes du sol est détruit. Dans un champ sans labour, des niveaux élevés de MOS constituent des réserves de nutriments du sol qui sont lentement libérés dans les sols. L’ajout d’une culture de couverture vivante dans un champ sans labour augmente la matière organique active (sucres et protéines) pour les microbes du sol. Les microbes du sol peuvent se nourrir de deux cultures au lieu d’une seule par an. Les microbes prospèrent dans des conditions de culture sans labour et dans les cultures de couverture hivernales. Les cultures de couverture et le fumier peuvent être utilisés pour nourrir les microbes du sol et recycler les éléments nutritifs du sol. À mesure que les microbes du sol décomposent les résidus organiques, ils libèrent lentement des éléments nutritifs dans le sol pour les cultures de couverture hivernales ou pour la culture précédente. Les cultures de couverture empêchent la perte de nutriments par l’érosion du sol, le lessivage, la volatilisation ou la dénitrification.
Résumé
Les micro-organismes abondent dans le sol et jouent un rôle essentiel dans la décomposition des résidus organiques et le recyclage des éléments nutritifs du sol. Les bactéries sont les microbes les plus petits et les plus résistants du sol et peuvent survivre dans des conditions difficiles comme le travail du sol. Les bactéries ne sont efficaces qu’à 20 à 30 pour cent pour recycler le carbone, ont une teneur élevée en azote (3 à 10 atomes de carbone pour 1 atome d’azote ou 10 à 30 pour cent d’azote), une teneur en carbone plus faible et une durée de vie courte. L’efficacité de l’utilisation du carbone est de 40 à 55 pour cent pour les champignons mycorhiziens, de sorte qu’ils stockent et recyclent plus de carbone (rapport carbone/azote de 10 : 1) et moins d’azote (10 pour cent) dans leurs cellules que les bactéries. Les champignons sont plus spécialisés mais ont besoin d’une source de nourriture constante et se développent mieux dans des conditions sans labour.
La matière organique du sol (MOS) est composée des fractions « vivantes » (micro-organismes), « mortes » (résidus frais) et « très mortes » (humus). La SOM active est composée de matières végétales ou animales fraîches qui servent de nourriture aux microbes et est composée de sucres et de protéines faciles à digérer. La SOM passive est résistante à la décomposition par les microbes (plus riche en lignine). Active SOM améliore la structure du sol et retient les nutriments disponibles pour les plantes. Chaque 1 pour cent de SOM contient 1 000 livres d’azote, 100 livres de phosphore, 100 livres de potassium et 100 livres de soufre ainsi que d’autres nutriments végétaux essentiels. Le travail du sol détruit la MOS en oxydant la MOS, permettant aux bactéries et autres microbes de décomposer rapidement les résidus organiques. Des températures et une humidité plus élevées augmentent la destruction de la MOS en augmentant les populations microbiennes dans le sol. Les résidus organiques avec un faible rapport carbone/azote (C:N) (inférieur à 20) se décomposent facilement et les nutriments sont rapidement libérés (4 à 8 semaines), tandis que les résidus organiques avec un rapport C:N élevé (supérieur à 20) se décomposent. lentement et les microbes vont capter l’azote du sol pour décomposer les résidus. Les protozoaires et les nématodes consomment d’autres microbes présents dans le sol et libèrent de l’azote sous forme d’ammonium, qui devient disponible pour d’autres micro-organismes ou est absorbé par les racines des plantes.
Reconnaissance
Cette fiche d’information a été réalisée en collaboration avec le Midwest Cover Crops Council (MCCC).
Les références
Alexandre, Martin. 1991. Introduction à la microbiologie des sols, 2e éd. Malabar, Floride : Société d’édition Krieger.
Ingham, Elaine R. 2014. «L’introduction à la biologie des sols». En biologie des sols . Service de conservation des ressources naturelles. PDF.
envirothonpa.org/wp-content/uploads/2014/04/7-Soil-Biology-Primer.pdf.
Magdoff, F. et H. van Es. 2001. Construire des sols pour de meilleures récoltes , 2e éd. Beltsville, MD : Réseau d’agriculture durable.